Anvisa autoriza a importação de 6 milhões de doses da vacina Coronavac
O aval, porém, não indica que as doses poderão ser aplicadas. Isso ainda dependerá do resultado dos testes clínicos e do registro da vacina no país.
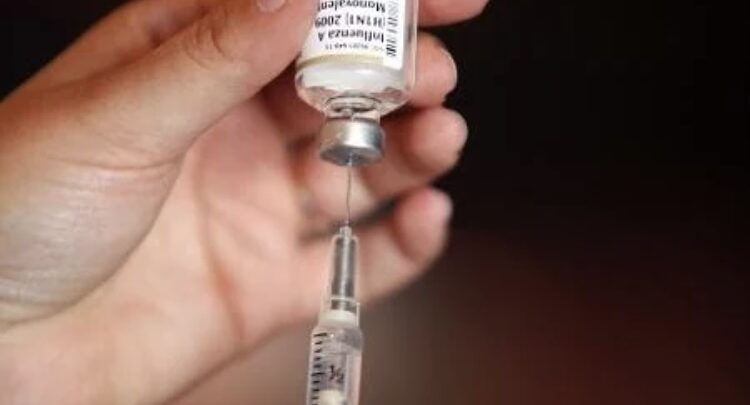
A Anvisa (Agência Nacional de Vigilância Sanitária) autorizou sexta-feira (23) a importação excepcional, pelo Instituto Butantan, de 6 milhões de doses da vacina Coronavac, produzida pela empresa chinesa Sinovac.
O aval, porém, não indica que as doses poderão ser aplicadas. Isso ainda dependerá do resultado dos testes clínicos e do registro da vacina no país.
A decisão ocorre um dia após o diretor-geral do instituto, Dimas Covas, afirmar que a Anvisa estaria retardando a autorização para a importação excepcional de matéria-prima da Sinovac que possibilitará a fabricação da vacina no Brasil.
O plano original do Butantan era receber, em outubro, 6 milhões de doses do imunizante Coronavac já prontos e fabricar no Brasil, até dezembro, as outras 40 milhões de doses a partir da matéria-prima que chegaria da China.
O pedido formal de liberação excepcional da importação de matéria-prima foi feito em 23 de setembro. Covas disse que, na quinta (22), recebeu a informação de que o assunto só será tratado em uma reunião em 11 de novembro. “Uma liberação que ocorre em dois meses deixa de ser excepcional”, afirmou ele.
Nesta semana, o presidente Jair Bolsonaro esvaziou o plano do Ministério da Saúde de compra futura de doses da Coronavac, criticou o governador João Doria (PSDB-SP) e disse que a vacina não seria confiável por causa de sua origem.
Inicialmente, a Anvisa não respondeu sobre os motivos do atraso e informou apenas que o processo passou a ser incluído em uma ferramenta especial de análise, chamado de circuito deliberativo, com previsão de decisão em até cinco dias.
Nesta sexta, a Anvisa negou ter atrasado a análise e afirmou que o processo já havia sido analisado, mas que “foram identificadas discrepâncias”. O órgão não disse quais.
A análise sobre a importação da matéria-prima deve ocorrer em reunião no dia 4 de novembro. “Cabe ressaltar que esse processo se encontrava pautado para o dia 4 de novembro, justamente para que houvesse tempo hábil para o atendimento das discrepâncias apontadas no processo referente à matéria-prima vacinal”, diz a Anvisa.







